بسمه تعالی
آزمایشگاه شیمی آلی3
آزمایش 1(واکنش دیلز آلدر)
مقدمه:
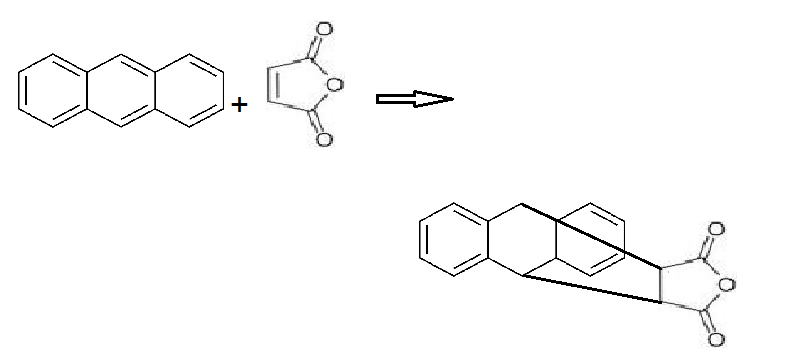
معمولا در اثر افزایش ترکیبات غیر اشباعی(کربونیل و سیانور) در موقعیت آلفا و بتا به موقعیت 1،4 ترکیبات مزدوج (مثل 1،3 بوتا دی ان) با تشکیل حلقه ی 6 عضوی واکنش دیلز آلدر انجام می شود.ترکیبات دی اتیلنی یا استیلنی را دی انوفیل می نامند و معرف دیگر را دی ان و محصول را آداکت (محصول افزایشی)می نامند.مکانیسم واکنش دیلز آلدر رادیکالی است ولی گاهی مکانیسم قطبی نیز پیشنهاد می شود.
واکنش دیلز –آلدر واکنشی است که در آن یک آلکن با یک دی ان مزدوج (۱و۳-دی ان) واکنش می دهد و مشتقی از سیکلو هگزن ایجاد می کند.به آلکن معمولا دی ان دوست یا دی انوفیل می گویند.واکنش اتیلن با بوتا دی ان منجر به تشکیل سیکلو هگزن می شود.
واکنش دیلز – آلدر یکی از مهمترین روش های سنتزی است که در دسترس شیمیدانان آلی است.چنانچه بجای آلکن از یک آلکین استفاده شود و مشتقی از ۱ و ۴ سیکلوهگزا دی ان بدست می آید.
واکنش دیلز – آلدر روشی بسیار مناسب برای تشکیل پیوند کربن – کربن و ترکیبات حلقوی شش ضلعی می باشد.در این واکنش پیوندهای کربن –کربن دارای پیوند π در دی انوفیل ازیک طرف و کربنهای ۱ و ۴ –دی ان از طرف دیگر تشکیل می شود بنابراین روی هم رفته دی انوفیل به صورت ۱ و ۴ به دی ان افزایش می یابد.بنابراین پیوندهای دوگانه مزدوج علاوه بر واکنش های معمولی آلکنها مانند افزایش الکترون دوستی در واکنشی دیگر یعنی واکنش دیلز – آلدر نیز شرکت می کنند.این تبدیل که به حلقه افزایی دیلز –آلدر معروف است پیوندهای جدید همزمان و به صورت فضا ویژه تشکیل می شوند. با توجه به اینکه ایجاد کربنهای کایرال امری نه چندان آسان در سنتزهای آلی می باشند، توانایی این واکنش در تشکیل راحت ترکیبات با مراکز نامتقارن اهمیت این دسته از واکنش ها را دو چندان می نماید. از جمله دی انهای مورد استفاده در کاربردهای واکنش دیلز – آلدر ترکیبات حلقوی سولفوردار می باشد. در سالهای اخیر مطالعات زیادی روی ترکیبات حلقوی سولفوردار جهت سنتز ترکیبات مختلف شده است. در این میان ترکیبات حلقوی سولفوردار H 2- تیوپیران -۴- اًُن از اهمیت خاصی برخوردار می باشند. اهمیت این ترکیبات از آنجا ناشی می شود که با استفاده از واکنش دیلز – آلدر این ترکیبات می توان بر محدودیت اساسی واکنش های دیلز – آلدر یعنی واکنش پذیری کم یا عدم واکنش پذیری دی انهای سیس غلبه نمود. دی انهای سیس اغلب هیچ محصول افزایشی در واکنش با دی انوفیلها تولید نمی کنند ولی در عوض دی انهای ترانس هزار برابر فعالتر از دی انهای مشابه سیس می باشند. این عدم واکنش پذیری مربوط به ازدحام فضایی موجود در دی انهای سیس می باشد. یک استراتژی مناسب جهت فائق آمدن بر این مشکل، استفاده ازH 2- تیوپیران -۴- ان می باشد. اولین بار گروه پروفسور Ward و همکارانش از کانادا موفق به انجام واکنش های دیلز – آلدر با استفاده از این ترکیبات به عنوان جانشینان مناسب دی انهای سیس شدند.
این گروه با انجام واکنش دیلز – آلدر بین دی هیدروتیوپیران -۴-ان با دی انوفیلهای خاص و در ادامه سولفورزدایی محصولات، موفق به شناسایی محصولاتی شدند که هم ارز با محصولات دیلز – آلدر حاصل از دی انهای سیس که توانایی شرکت در واکنش دیلز – آلدر را نداشتند، می باشند.با توجه به اهمیت این واکنشها، بر آن شدیم که در این پژوهش به ادامه مطالعات بپردازیم و سنتز ترکیبات جدیدی از این نوع را انجام دهیم.
نکته1:واکنش دیلز آلدر به طور کلی یک واکنش پیش بوده و موقعیت گروهها (استخلاف ها)در محصول افزایشی دست نخورده باقی می ماند.
نکته2:گروههای جاذب بر روی دی انوفیل می تواند سرعت واکنش را افزایش دهد.
روش های خشک کردن تولوئن:
برای خشک کردن 500 سی سی از این محلول حدود 5 گرم سدیم را به صورت نوار در می آوریم و به صورت ذره ذره وارد حلال می کنیم و سپس به آن 50 میلی گرم شناساگر بنزوفنون اضافه می کنیم و رفلاکس می کنیم به محض تشکیل محلول بنفش تمام آب موجود در آن خشک شده و مطمئن می شویم که حلالها کاملا خشک شده و محلول را تقطیر می کنیم.
نکته: نقش سنگ جوش برای جلوگیری از پاشیده شدن محلول به اطراف است.
مواد و وسایل مورد نیاز:انیدرید مالئیک،آنتراسن،زایلن خشک(یا تولوئن)،شاربن(زغال سنگ)،بالن ته گرد،مبرد،قیف بوخنر،دسیکاتور خلاء
روش کار:در یک بالن ته گرد 50 میلی گرم آنتراسن خالص قرار داده و 0.55 گرم انیدرید مالئیک و 10 میلی لیتر تولوئن افزوده و به مدت 25 دقیقه آن را رفله کنید و در 10 دقیقه اول گهگاهی آن را تکان دهید وبعد از اتمام زمان واکنش بگذارید سرد شود و 0.25 گرم شاربن به آن بیفزایید و 5 دقیقه بجوشانید و محلول داغ را صاف کنید.جامد در اثر سرد کردن جدا می شود با قیف بوخنر جدا کنید و در دسیکاتور خلاء خشک کنید تا زایلن اضافی جذب گردد.راندمان 1.1 گرم آداکت با نقطه ذوب 262_263 درجه سانتی گراد و بی رنگ می باشد که قابل تجزیه است. محصول را در یک لوله آزمایش قرار دهید و درب آن را محکم ببندید،زیرا در برابر هوا قسمت انیدریدی مولکول هیدراته می شود.


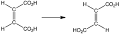 آزمایش ایزومراسیون
آزمایش ایزومراسیون